Questões de Concurso
Filtrar
145 Questões de concurso encontradas
Página 20 de 29
Questões por página:
Questões por página:
A análise elementar quantitativa de 2,035 g de um composto orgânico oxigenado X forneceu 4,840 g de CO2 e 2,475 g de H2 O, por combustão. Verficou-se também que a referida massa de X ocupa um volume de 1,1275 L, a 227°C e 1atm de pressão. Dentre todos os possíveis isômeros, X é o único que possui enantiômeros. O número total de isômeros (constitucionais e estereoisômeros) com a fórmula molecular em questão e o nome do composto X estão respectivamente indicados em:
Uma amostra de 0,265 g de um antibiótico em pó foi dissolvida em HCl e completou-se o volume até 100,00 mL de solução. Uma alíquota de 25,00 mL foi transferida para um balão, seguida da adição de 25,00 mL de solução aquosa 0,018 mol.L–1 de KBrO3. Um excesso de KBr foi adicionado para formar Br2, segundo a equação a seguir: BrO3– + 5Br – + 6H+ → 3Br2 + 3H2O
O bromo formado reage com toda a sulfanilamida presente no antibiótico e, após um tempo, é adicionado excesso de KI, para reagir com o excesso de bromo, formando I2. Finalmente, o iodo formado é titulado, consumindo 13,00 mL de uma solução aquosa 0,12 mol.L–1 de tiossulfato de sódio. As demais equações químicas são:
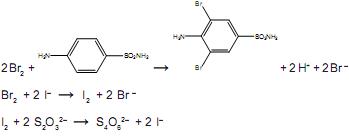
A porcentagem de sulfanilamida presente na amostra do antibiótico em pó é aproximadamente igual a:
Dado: Massa molar da sulfanilamida= 172 g. mol -1
Quando uma amostra de 4,0 g de bicarbonato de sódio (NaHCO3) é posta em contato com acido clorídrico (HCl), libera 0,96 L de CO2, medido a 273 K e 1 atm? A equação que descreve a reação é a seguinte: NaHCO3 + HCl → NaCl + H2O + CO2 Podemos afirmar que o grau de pureza da amostra de bicarbonato de sódio é
A reação de Sabatier envolve a reação do hidrogênio com o dióxido de carbono em temperaturas e em pressões elevadas na presença de um catalisador de níquel, cujo resultado final é metano e água. A reação de Sabatier é descrita pela seguinte equação: CO2 (g) + 4 H2 (g) 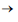 CH4 (g) + 2 H2O(l)
CH4 (g) + 2 H2O(l)
Esta reação, descoberta pelo químico francês Paul Sabatier, tem sido estudada para remover CO2 de atmosferas artificiais como em espaçonaves. Considerando que um indivíduo libere para o ambiente 0,6 kg de dióxido de carbono por dia, e que 80% desse gás será removido pelo processo de Sabatier, a massa de metano produzida por dia é de Dados: Massas Molares: H = 1g.mol-1 C = 12g.mol-1 O=16g.mol-1
 CH4 (g) + 2 H2O(l)
CH4 (g) + 2 H2O(l) Esta reação, descoberta pelo químico francês Paul Sabatier, tem sido estudada para remover CO2 de atmosferas artificiais como em espaçonaves. Considerando que um indivíduo libere para o ambiente 0,6 kg de dióxido de carbono por dia, e que 80% desse gás será removido pelo processo de Sabatier, a massa de metano produzida por dia é de Dados: Massas Molares: H = 1g.mol-1 C = 12g.mol-1 O=16g.mol-1
Em um laboratório foi montada uma aparelhagem para recolhimento do gás oxigênio produzido na reação de decomposição do clorato de potássio, como ilustra a figura a seguir.
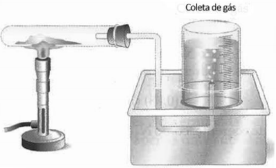
A reação observada pode ser representada pela equação: 2 KClO3 → 2 KCl + 3 O2 Uma amostra de clorato de potássio foi parcialmente decomposta sendo a pressão do gás recolhido de 0,8 atm e seu volume de 180 mL na temperatura de 27ºC. Considerando o comportamento ideal do gás, a massa de clorato de potássio que sofreu decomposição foi de, aproximadamente, Dados: Massa Molar: KClO3 = 122,5 g.mol-1 Constante real dos gases R= 0,082atm.L.mol-1 .K-1

A reação observada pode ser representada pela equação: 2 KClO3 → 2 KCl + 3 O2 Uma amostra de clorato de potássio foi parcialmente decomposta sendo a pressão do gás recolhido de 0,8 atm e seu volume de 180 mL na temperatura de 27ºC. Considerando o comportamento ideal do gás, a massa de clorato de potássio que sofreu decomposição foi de, aproximadamente, Dados: Massa Molar: KClO3 = 122,5 g.mol-1 Constante real dos gases R= 0,082atm.L.mol-1 .K-1