Filtrar
23 Questões de concurso encontradas
Página 1 de 5
Questões por página:
Questões por página:
Concurso:
Prefeitura de Gravataí - RS
Disciplina:
Engenharia Química e Química Industrial
Sobre o conceito de barreiras aplicado à segurança de alimentos, assinale a alternativa correta.
Concurso:
Prefeitura de Nova Olímpia - PR
Disciplina:
Engenharia Química e Química Industrial
Todos os produtos de higiene pessoal a seguir são industrializados e produzidos sob responsabilidade de um químico, EXCETO:
Concurso:
IDEMA-RN
Disciplina:
Engenharia Química e Química Industrial
Preencha as lacunas e assinale a alternativa correta.
O Rio Grande do Norte se consolida como um dos principais protagonistas da transição energética no Brasil, destacando-se pela expressiva produção de energia eólica e solar, impulsionada por condições naturais privilegiadas. Além de liderar a geração eólica no país, o estado também desponta na adoção de novas tecnologias sustentáveis, com destaque para os investimentos em fontes power-to-X, como: _________ e ____________ verdes.
Concurso:
CONAB
Disciplina:
Engenharia Química e Química Industrial
Relacione CORRETAMENTE as técnicas de análise de risco com suas características, numerando a Coluna II de acordo com a Coluna I.
COLUNA I
1. AMFE. 2. HAZOP. 3. AAF.
COLUNA II
(__)Identifica riscos e desvios de parâmetros de processos.
(__)É dedutiva e utiliza um evento topo e constrói níveis subsequentes identificando falhas.
(__)Identifica os modos de falhas dos componentes de um sistema e seus efeitos.
A sequência CORRETA da correlação entre as colunas é:
COLUNA I
1. AMFE. 2. HAZOP. 3. AAF.
COLUNA II
(__)Identifica riscos e desvios de parâmetros de processos.
(__)É dedutiva e utiliza um evento topo e constrói níveis subsequentes identificando falhas.
(__)Identifica os modos de falhas dos componentes de um sistema e seus efeitos.
A sequência CORRETA da correlação entre as colunas é:
Concurso:
Prefeitura de Santos
Disciplina:
Engenharia Química e Química Industrial
A queima de combustíveis à base de Carbono, na presença de Oxigênio atmosférico, foi talvez a primeira tecnologia da engenharia química desenvolvida pelo ser humano. Quando dominamos o fogo, milênios antes de entendermos os princípios científicos envolvidos, aprendemos a reproduzir comportamentos empíricos e a contornar as dificuldades que apareciam, nos forçando a ser uma espécie cada vez mais criativa. Seguramente não foram poucos os dias de vento e chuva, onde os ancestrais humanos tiveram de usar musgo, cera das cascas de frutas e óleo de folhas de coníferas para aproveitar as chispas do novo conhecimento. Muito tempo se passou, a chama do conhecimento cresceu ainda mais e a humanidade decidiu explorar o espaço. Novamente, se deparou com dificuldades impensadas até então. Agora precisamos queimar metais (para obter maiores quantidades de energia) e levantar foguetes até superar a atmosfera terrestre. Exatamente lá onde não temos o oxigênio nos esperando com nossa fagulha de atrevimento. Mas encontramos soluções, como sempre fazemos.
Os poderosos combustíveis sólidos foram adotados inicialmente pela NASA em seus lançamentos e agora também sendo usados pelas agências privadas que prestam serviços aos governos, levando carga e passageiros para suas missões fora do planeta. As reações a seguir, representam as duas principais reações de oxirredução envolvidas na queima dos combustíveis sólidos dos foguetes:
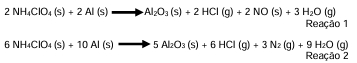
Analisando ambas as reações combinadas, fica evidente que o alumínio passa do estado de oxidação (zero) para (3+), enquanto o cloro passa de (+7) para (-1). Assim, pode-se concluir nessa análise que o estado de oxidação de nitrogênio vai de
Os poderosos combustíveis sólidos foram adotados inicialmente pela NASA em seus lançamentos e agora também sendo usados pelas agências privadas que prestam serviços aos governos, levando carga e passageiros para suas missões fora do planeta. As reações a seguir, representam as duas principais reações de oxirredução envolvidas na queima dos combustíveis sólidos dos foguetes:
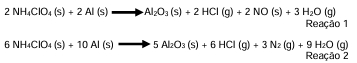
Analisando ambas as reações combinadas, fica evidente que o alumínio passa do estado de oxidação (zero) para (3+), enquanto o cloro passa de (+7) para (-1). Assim, pode-se concluir nessa análise que o estado de oxidação de nitrogênio vai de