Questões de Concurso
Filtrar
11 Questões de concurso encontradas
Página 2 de 3
Questões por página:
Questões por página:
Três frascos foram encontrados sem rótulo na bancada de um laboratório. Um deles continha solução de KOH a 0,1 mol/L; o outro, solução de CaCl2 a 0,05 mol/L; e o outro, solução de CH3CH2COOH a 0,1 mol/L. Na tentativa de identificar a solução contida em cada um deles, um técnico usou volumes iguais das soluções dos frascos para medir a pressão de vapor sob mesma temperatura, utilizando um sistema adequado. Os resultados obtidos estão indicados pelos ponteiros dos manômetros nesta figura.
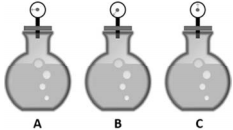
Com base nas informações e na figura apresentadas, é correto afirmar que os frascos identificados por A, B e C contêm, respectivamente, as soluções de
A presença do soluto não volátil pode modificar algumas propriedades físicas das soluções, em comparação às mesmas propriedades do solvente puro. Essas mudanças dependem fundamentalmente das quantidades relativas das partículas dissolvidas e do solvente. Ao comparar as temperaturas de fusão e ebulição da água pura e de uma solução aquosa de NaCl, é possível esperar
Correlacione as importantes propriedades da água (enumeradas de 1 a 8) com suas respectivas funções no transporte de espécies entre os compartimentos litosfera, hidrosfera e atmosfera durante o ciclo hidrológico. Após a correta correlação, assinale a alternativa correta: 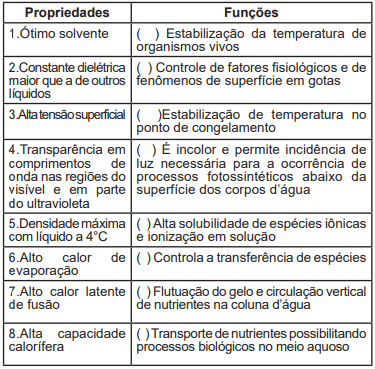
Assinale a alternativa que corresponde à ordem correta das correlações das propriedades com as funções, de cima para baixo segundo o que foi preenchido no quadro anterior:

Assinale a alternativa que corresponde à ordem correta das correlações das propriedades com as funções, de cima para baixo segundo o que foi preenchido no quadro anterior:
pressão de vapor de qualquer substância líquida ou sólida depende do tipo de interações entre as partículas. Quanto mais forte for a ligação entre os átomos, maior será a pressão de vapor da substância. Dados os compostos PH3, NH3, BiH3 e SbH3 a ordem decrescente de pressão de vapor será:
Adicionar sal de cozinha ao gelo é uma prática comum quando se quer “gelar” bebidas dentro da geleira. A adição do sal faz com que a temperatura de fusão se torne inferior à da água pura.
(Dados: Kf = 1,86 ºC.kg.mol-1 ; M(g.mol-1 ): Cl = 35,5; Na = 23)
A diferença na temperatura de fusão (em °C) na mistura obtida ao se dissolver 200 g de sal de cozinha em 1 kg de água, em relação à água pura, é de:
(Dados: Kf = 1,86 ºC.kg.mol-1 ; M(g.mol-1 ): Cl = 35,5; Na = 23)
A diferença na temperatura de fusão (em °C) na mistura obtida ao se dissolver 200 g de sal de cozinha em 1 kg de água, em relação à água pura, é de: