Questões de Concurso
Filtrar
82 Questões de concurso encontradas
Página 15 de 17
Questões por página:
Questões por página:
mostrar texto associado
O indicador vermelho de fenol apresenta cor amarela em soluções aquosas de pH < 6,4, e, cor vermelha, em soluções aquosas de pH > 8,2. Na água pura (pH = 7,0), esse indicador apresenta cor laranja.
A uma amostra de água pura foi acrescentado o indicador vermelho de fenol. Em seguida, foi acrescentado certo óxido que mudou a cor apresentada por esse indicador de laranja para amarela. Esse óxido pode ter sido o
Um certo metal (M), de massa molar igual a 48 g mol-1, forma um sal de cloreto bastante reativo, que em água sofre hidrólise e produz o óxido desse metal. Verificou-se que na composição de 80 g do óxido,48 g correspondem a massa apenas do metal. (Dado: massa molar do oxigênio igual a 16 g mol-1 )
A fórmula mínima desse óxido é:
A fórmula mínima desse óxido é:
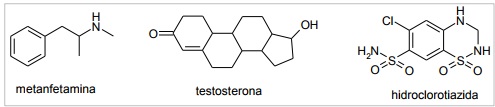
Sobre as substâncias utilizadas em doping, apresentadas na questão anterior, considere as seguintes afirmativas:
1. A metanfetamina possui uma amina secundária.2. A testosterona é um composto aromático.
3. A testosterona possui função cetona.4. A hidroclorotiazida é um sal.
Assinale a alternativa correta.
Uma prova de que a química está presente em nosso cotidiano é a presença de compostos químicos nos mais diversos produtos, que pensamos vê-los somente nos livros. Alguns exemplos são o leite de magnésia composto pelo Mg(OH)2; a água de bateria, que contém o H2SO4, e vitaminas compradas em farmácia que podem conter o FeSO4.
Marque a alternativa que apresenta corretamente a nomenclatura dos compostos citados, de acordo com a sequência mencionada no texto:
Marque a alternativa que apresenta corretamente a nomenclatura dos compostos citados, de acordo com a sequência mencionada no texto: