Questões de Concurso
Filtrar
62 Questões de concurso encontradas
Página 8 de 13
Questões por página:
Questões por página:
Considerando as reações a seguir:
 .
.
 ,
,
OΔH da reação a seguir é igual a:
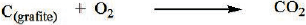 .
.
Questão Anulada
O ΔH0 da reação mostrada abaixo é igual a :
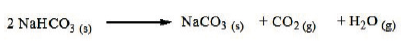
Dados:
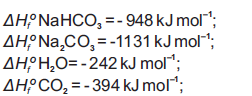
O ácido benzoico tem entalpia padrão de combustão igual a -3227 kJ.mol -1 . Para calibrar um calorímetro, foram usados 2,27 g deste ácido, aumentando em 5,0°C a temperatura do calorímetro. Em seguida, com o calorímetro a 25°C, promoveu-se a queima de 1,6 g de acetileno (etino) e a temperatura subiu para 31,7°C. A entalpia padrão de combustão do acetileno, em kJ.mol -1 , é aproximadamente igual a:
Dados: Massas molares (g.mol -1 ), H= 1, C=12, O=16
Dados: Massas molares (g.mol -1 ), H= 1, C=12, O=16
As Leis da Termodinâmica explicam as variações de energia e a tendência de ocorrência dos processos de modo espontâneo, sendo essenciais para a compreensão da Química. Considerando, por exemplo, um processo que é exotérmico, em relação à espontaneidade, à variação de entropia (ΔS) e à temperatura, pode-se afirmar que:
Os valores de E° para os pares (piruvato/lactato) e (NAD+/NADH) em pH 7 e 25°C são -0,19 V e - 0,32 V, respectivamente. Na redução enzimática do piruvato a lactato (2 elétrons por molécula) por NADH (2 elétrons por molécula), então, o valor de ΔE° para a reação e o ΔG° em pH 7, por mol de piruvato reduzido, são respectivamente: (Dado: F= 96500 C/Mol) A reação pode ser escrita como: Piruvato + NADH ⇔ lactato + NAD+