Questões de Concurso
Filtrar
62 Questões de concurso encontradas
Página 9 de 13
Questões por página:
Questões por página:
O dióxido de nitrogênio e o óxido nítrico são poluentes primários considerados relevantes no que diz respeito à poluição atmosférica. Juntos, esses dois compostos são considerados as moléculas mais importantes da química da atmosfera. Alguns autores também incluem nessa lista o N2O que, apesar de não ser importante enquanto poluente da troposfera, acaba por exercer grande influência na estratosfera, no que diz respeito ao desequilíbrio do efeito estufa. As reações a seguir apresentam as reações de combustão de alguns óxidos de nitrogênio.2NO(g) + O2 (g) 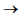 2NO2 (g)
2NO2 (g) 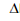 H1 2N2O(g) + 3O2 (g)
H1 2N2O(g) + 3O2 (g) 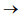 4NO2 (g)
4NO2 (g) 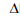 H2
H2
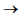 2NO2 (g)
2NO2 (g) 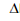 H1 2N2O(g) + 3O2 (g)
H1 2N2O(g) + 3O2 (g) 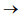 4NO2 (g)
4NO2 (g) 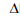 H2
H2 Muitas reações envolvem o ganho ou a perda de energia e são chamadas de reações endotérmicas ou exotérmicas. Para o estudo quantitativo desta variação de energia utilizamos ΔH, que é igual à quantidade de calor trocado à pressão constante. Nesse estudo, foram formuladas três leis conhecidas como Leis da Termodinâmica; analise-as.
I. O valor de ΔH é diretamente proporcional à quantidade de reagente ou produto, desde que não haja reagente limitante.
II. O ΔH para uma reação é igual em módulo, mas de sinal contrário ao ΔH da reação inversa, ou seja, a quantidade de calor liberado e a de calor recebido são iguais.
III. O valor de ΔH para uma reação é o mesmo, seja a reação direta ou em etapas.
Corresponde(m) às Leis da Termodinâmica apenas
Para um certo líquido, o ponto normal de ebulição é 400 K. O calor de vaporização pode ser calculado pela equação: ΔH = 13500 -10 T (cal mol-1). Admitindo que seu vapor se comporte como gás ideal e que o volume do líquido seja desprezível quando comparado com o do vapor, os valores aproximados de q, w, ΔU, ΔH, ΔS e ΔG, para o processo de vaporização de 1 mol de benzeno a 400 K são:
Dado: 1 cal = ~4,187 J
Dado: 1 cal = ~4,187 J
O estudo sobre a espontaneidade de uma reação é um tema de extrema importância no estudo da química. Para essa análise, são consideradas as variáveis de estado entalpia, entropia e energia livre. Sendo assim, à pressão e temperatura constantes, um processo será espontâneo se apresentar