Questões de Concurso
Filtrar
26 Questões de concurso encontradas
Página 2 de 6
Questões por página:
Questões por página:
Um mol de um gás monoatômico ideal, que está inicialmente a uma temperatura To, sofre uma transformação isovolumétrica, de modo que a sua pressão triplica. Em seguida, o gás sofre uma nova transformação isotérmica, de modo que o seu volume dobra de valor nesta transformação. A quantidade de calor que o gás recebeu ao longo de todo o processo é igual a: Obs.: considere R a constante geral dos gases.
Um gás sofre uma expansão sem variar sua pressão. Nessa situação o gás sofre uma transformação chamada de:
Disciplina:
Física
O gráfico indica o fator de compressibilidade à temperatura constante do gás hidrogênio de acordo com seu comportamento real na relação P?V/nR?T em função da pressão.
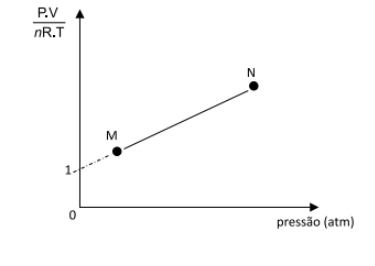
Caso o gás hidrogênio se comportasse como um gás ideal, a reta seria
Um sistema gasoso com n moles de um gás ideal dobra o seu volume num processo isotérmico. Considerando que isto acontece a temperatura T e que R é a Constante Universal dos Gases, a variação de Entropia é igual a
Concurso:
Universidade Federal Fluminense (UFF)
Disciplina:
Física
Um material passa do estado sólido para gasoso e de gasoso para líquido se houver: