Concurso:
MPU
Disciplina:
Engenharia Química
mostrar texto associado
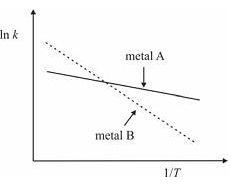
A energia de ativação da reação de hidrogenação catalisada pelo metal B é superior à da reação catalisada pelo metal A.
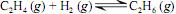
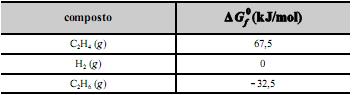
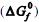 a 25 ºC de cada composto envolvido.
a 25 ºC de cada composto envolvido.