Questões de Concurso
Filtrar
1.178 Questões de concurso encontradas
Página 18 de 236
Questões por página:
Questões por página:
A força de um ácido está diretamente ligada a sua capacidade de sofrer ionização. Essa força pode ser determinada experimentalmente e expressa a partir do valor da constante de ionização ácida (Ka).
Observe a tabela a seguir que contém os valores de pKa para cinco ácidos inorgânicos distintos.
ÁCIDO pKa carbônico 6,37 hipocloroso 7,53 hipobromoso 8,69 bórico 9,14 cianídrico 9,31
O ácido mais forte é o
Observe a tabela a seguir que contém os valores de pKa para cinco ácidos inorgânicos distintos.
ÁCIDO pKa carbônico 6,37 hipocloroso 7,53 hipobromoso 8,69 bórico 9,14 cianídrico 9,31
O ácido mais forte é o
Quando uma ligação química se forma, os átomos rearrumam seus elétrons de modo a atingirem a configuração eletrônica de um gás nobre. A esse princípio, o químico norte-americano G. N. Lewis deu o nome de Regra do Octeto. No entanto, hoje sabemos que diversos compostos não obedecem a esse princípio. Um exemplo de composto que viola esse princípio é o
Um experimento de cinética química bastante conhecido é chamado de “reação relógio”. Nele, os íons persulfato reagem com íons iodeto conforme a reação balanceada a seguir.
S2O8 2 – (aq) + 3 I – (aq) → 2 SO4 2 – (aq) + I3 – (aq)
A tabela a seguir contém dados experimentais sobre a reação em condições específicas de temperatura e pressão.
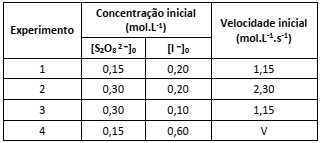
A partir das informações apresentadas é possível prever que a velocidade (V) do Experimento 4 será
S2O8 2 – (aq) + 3 I – (aq) → 2 SO4 2 – (aq) + I3 – (aq)
A tabela a seguir contém dados experimentais sobre a reação em condições específicas de temperatura e pressão.

A partir das informações apresentadas é possível prever que a velocidade (V) do Experimento 4 será
Desde o início do século XX ficou claro que a mecânica clássica não seria capaz de explicar a estrutura interna dos átomos. Novas leis precisaram ser desenvolvidas e ficaram conhecidas como mecânica quântica.
A partir dessas novas leis foi possível determinar a(o)
A partir dessas novas leis foi possível determinar a(o)
Os mono-nitrofenóis (estruturas a seguir) têm diversas aplicações industriais, sendo usados, por exemplo, como intermediários na síntese de corantes e pesticidas organofosforados.
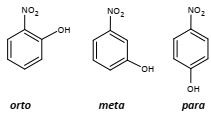
Apesar de serem isômeros entre si, eles possuem diferentes pontos de ebulição. Dentre eles, o composto de menor ponto de ebulição é o isômero

Apesar de serem isômeros entre si, eles possuem diferentes pontos de ebulição. Dentre eles, o composto de menor ponto de ebulição é o isômero