Questões da prova:
Instituto Consulplan - 2023 - Instituto Federal Pará - TAE - Técnico de Laboratório - Ciências do Solo
limpar filtros
70 Questões de concurso encontradas
Página 6 de 14
Questões por página:
Questões por página:
Concurso:
Instituto Federal Pará
Disciplina:
Química
Considere uma solução de soro fisiológico 0,9 % m/v de NaCl. Se a solução for aquecida para a evaporação do solvente, o volume necessário de soro fisiológico para resultar em 3,2 g de NaCl será de:
Concurso:
Instituto Federal Pará
Disciplina:
Química
Quando o urânio-238 decai por emissão alfa, forma um elemento cujo número atômico constitui o tório (Th): 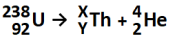
Considerando o exposto, os valores de X e Y (relativos ao tório) são, respectivamente:
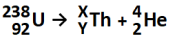
Considerando o exposto, os valores de X e Y (relativos ao tório) são, respectivamente:
Concurso:
Instituto Federal Pará
Disciplina:
Química
JM, técnico de laboratório, foi contratado por certa empresa siderúrgica para monitorar a produção de ferro a partir de minérios de ferro. O profissional observou a reação de redução do Fe2O3 pelo CO para produzir ferro metálico e CO2. Ao gerar o relatório detalhado de suas observações, JM precisou expressar a reação química ocorrida no referido processo da siderúrgica. A equação química não balanceada é apresentada a seguir:
Fe2O3(s) + CO(g) → Fe(s) + CO2(g)
Após o balanceamento, a somatória dos menores coeficientes estequiométricos (números inteiros) para a reação química apresentada será de:
Fe2O3(s) + CO(g) → Fe(s) + CO2(g)
Após o balanceamento, a somatória dos menores coeficientes estequiométricos (números inteiros) para a reação química apresentada será de:
Concurso:
Instituto Federal Pará
Disciplina:
Química
Ao preparar os materiais para a aula de reações químicas, o técnico de laboratório observou no roteiro a imagem e a descrição a seguir: 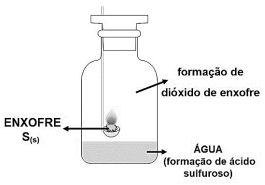
Certa quantidade de enxofre é inserida no dispositivo de combustão e a chama é iniciada no bico de Bunsen. Então, ainda com a chama acesa, o dispositivo é inserido em um frasco hermeticamente fechado e o dióxido de enxofre formado fica confinado no recipiente. Este gás, por sua vez, reage com a água contida no fundo do frasco, formando uma solução de ácido sulfuroso. Considerando todas as informações apresentadas e a imagem, a reação que expressa corretamente a formação do ácido sulfuroso é:

Certa quantidade de enxofre é inserida no dispositivo de combustão e a chama é iniciada no bico de Bunsen. Então, ainda com a chama acesa, o dispositivo é inserido em um frasco hermeticamente fechado e o dióxido de enxofre formado fica confinado no recipiente. Este gás, por sua vez, reage com a água contida no fundo do frasco, formando uma solução de ácido sulfuroso. Considerando todas as informações apresentadas e a imagem, a reação que expressa corretamente a formação do ácido sulfuroso é:
Concurso:
Instituto Federal Pará
Disciplina:
Química
A Tomografia por Emissão de Pósitrons (conhecida pela sigla inglesa PET) é uma técnica de cintilografia que utiliza radionuclídeos, os quais liberam partículas chamadas pósitrons em vez de fótons de alta energia, como na maioria dos outros tipos de cintilografia. O objetivo da PET é produzir imagens do interior do corpo para diagnosticar doenças como o câncer. Descreve corretamente um pósitron: