Questões da prova:
CESGRANRIO - 2024 - UNEMAT - MT - Químico
limpar filtros
60 Questões de concurso encontradas
Página 4 de 12
Questões por página:
Questões por página:
Uma solução foi formada a partir da mistura das seguintes soluções aquosas:
• 500 mL de solução de fluoreto de magnésio com concentração 0,020 mol L-1
• 200 mL de solução de fluoreto de alumínio com concentração 3,36 g L-1
• 300 mL de solução de fluoreto de sódio com concentração 0,060 mol L-1
Admitindo-se que os solutos estão completamente dissociados, a concentração de íons fluoreto, em mol L-1 , na solução resultante da mistura é igual a
Dado
Al = 27 g mol-1 F = 19 g mol-1
• 500 mL de solução de fluoreto de magnésio com concentração 0,020 mol L-1
• 200 mL de solução de fluoreto de alumínio com concentração 3,36 g L-1
• 300 mL de solução de fluoreto de sódio com concentração 0,060 mol L-1
Admitindo-se que os solutos estão completamente dissociados, a concentração de íons fluoreto, em mol L-1 , na solução resultante da mistura é igual a
Dado
Al = 27 g mol-1 F = 19 g mol-1
O níquel é um elemento de transição cujo principal íon é o Ni2+.
As configurações eletrônicas do átomo de níquel no estado fundamental e do íon Ni2+ correspondem, respectivamente, a
As configurações eletrônicas do átomo de níquel no estado fundamental e do íon Ni2+ correspondem, respectivamente, a
Um procedimento foi desenvolvido para a determinação de íons cálcio em uma solução aquosa. A uma alíquota de 200 mL dessa solução foi adicionado excesso de ácido oxálico (H2 C2 O4 ). Em seguida, adicionou-se amônia, de modo a precipitar todo o cálcio presente na amostra na forma de oxalato de cálcio. O precipitado foi filtrado, seco e calcinado, de acordo com a seguinte reação:
CaC2 O4 (s) → CaO (s) + CO (g) + CO2 (g)
Após o resfriamento, a massa de óxido de cálcio na amostra foi de 112 mg.
A concentração de íons cálcio, em g L-1, na solução aquosa é
Dado Ca = 40 g mol-1, C = 12 g mol-1, O = 16 g mol-1
CaC2 O4 (s) → CaO (s) + CO (g) + CO2 (g)
Após o resfriamento, a massa de óxido de cálcio na amostra foi de 112 mg.
A concentração de íons cálcio, em g L-1, na solução aquosa é
Dado Ca = 40 g mol-1, C = 12 g mol-1, O = 16 g mol-1
O sorbitol é um composto usado como adoçante em alimentos. Esse composto corresponde a um dos estereoisômeros do composto representado pela seguinte fórmula estrutural:
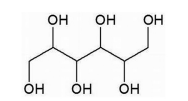
O número de átomos de carbono assimétrico no composto apresentado na fórmula estrutural é igual a

O número de átomos de carbono assimétrico no composto apresentado na fórmula estrutural é igual a
Uma rota industrial para a produção de metanol consiste na reação de adição entre monóxido de carbono e gás hidrogênio. Na reação de 8 kg de gás hidrogênio em excesso de monóxido de carbono, há formação de 48 kg de metanol.
A porcentagem de rendimento dessa reação é igual a
Dado H = 1 g mol-1, C = 12 g mol-1, O = 16 g mol-1
A porcentagem de rendimento dessa reação é igual a
Dado H = 1 g mol-1, C = 12 g mol-1, O = 16 g mol-1