70 Questões de concurso encontradas
Página 9 de 14
Questões por página:
As principais funções químicas – ácidos, bases, sais e óxidos – são encontradas em nosso cotidiano e também em nosso organismo. As teorias definidas para estas funções químicas são citadas a seguir.
• Segundo a teoria de Arrhenius, “um ácido é todo composto molecular que, em solução aquosa, se ioniza, produzido exclusivamente como cátion o 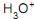 (hidroxônio) e que pode ser representado por
(hidroxônio) e que pode ser representado por 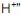 , e “uma base é um composto que em solução aquosa sofre dissociação iônica, produzindo íon hidroxila”.
, e “uma base é um composto que em solução aquosa sofre dissociação iônica, produzindo íon hidroxila”.
• Segundo a teoria de Brønsted-Lowry, “os ácidos são moléculas ou íons doadores de prótons” e “as bases são moléculas ou íons aceitadores de prótons”.
• Segundo a teoria de Lewis, “um ácido é um aceitador de par de elétrons”, e “uma base é um doador de par de elétrons”.
Com base nessas teorias, analise as afirmações abaixo.
I - 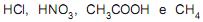 são considerados ácidos, e
são considerados ácidos, e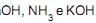 são considerados bases, segundo a teoria de Arrhenius.
são considerados bases, segundo a teoria de Arrhenius.
II - 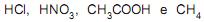 são considerados ácidos, e
são considerados ácidos, e 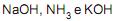 são considerados bases, segundo a teoria de Brønsted-Lowry.
são considerados bases, segundo a teoria de Brønsted-Lowry.
III - Na reação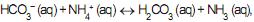 , o íon amônio
, o íon amônio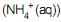 e o ácido carbônico
e o ácido carbônico 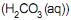 são considerados ácidos de Brønsted-Lowry, e as espécies
são considerados ácidos de Brønsted-Lowry, e as espécies  são bases de Lewis.
são bases de Lewis.
Está correto APENAS o que se afirma em
O abaixamento crioscópico do benzeno é utilizado na indústria do petróleo para medir massas molares de solutos. A equação que rege esse fenômeno pode ser expressa por: 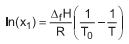
Sabe-se que:
• X1 é a fração molar de solvente em solução que cristaliza na temperatura T;
• ΔfH e T0 são, respectivamente, a variação de entalpia e a temperatura de fusão do solvente puro;
• R é a constante universal dos gases que pode ser aproximada por 2 cal/(mol•K);
• a variação de entropia de fusão do benzeno puro é 8 cal/(mol•K);
• a massa molar do benzeno é 78 g/mol;
• a temperatura de fusão do benzeno (T0) é 278,5 K.
A massa molar do soluto, a 278 K, necessária para a cristalização do benzeno a partir de uma solução de 10 g de soluto em 780 g de benzeno, em g/mol, é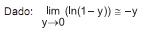
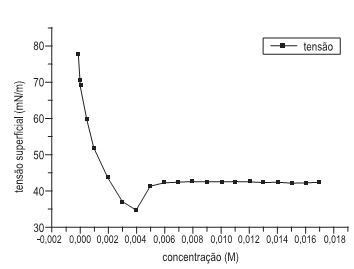
A figura acima apresenta dados experimentais de tensão superficial em função da concentração de surfactante (tenso-ativo) não iônico. Notam-se duas regiões distintas, uma de 0 a 0,003 M, e outra para concentrações acima de 0,005 M. A partir de uma análise, conclui-se que