Questões da prova:
IBFC - 2023 - Secretaria de Estado da Educação e do Esporte do Paraná (SEED-PR) - DOCÊNCIA DOS COMPONENTES CURRICULARES DA MATRIZ - QUÍMICA
limpar filtros
30 Questões de concurso encontradas
Página 3 de 6
Questões por página:
Questões por página:
Disciplina:
Química
“O metano dura bem menos na atmosfera que o CO2, mas sua capacidade de reter calor é 21 vezes maior; a do N2O é 310 vezes maior que a do CO2. O metano produzido no fundo dos oceanos pela decomposição de material orgânico, principalmente nas crateras, que chega à superfície marinha deve contribuir com algo entre 1% e 5% das emissões globais desse gás para a atmosfera, de acordo com uma estimativa do Instituto Max Planck de Microbiologia Marinha e do Centro de Ciências Ambientais Marinhas (Marum) da Universidade de Bremen, ambos da Alemanha, publicada em 2013 na Nature Geoscience”. (FIORAVANT1,2018).
Considerando a formação do metano, a partir da reação:
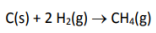
Assinale a alternativa que apresenta qual seria a quantidade em quilocalorias, em valor absoluto, envolvido na formação de 1 mol de metano dadas as seguintes variações de entalpia de combustão: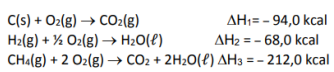
Assinale a alternativa correta.
Considerando a formação do metano, a partir da reação:
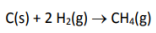
Assinale a alternativa que apresenta qual seria a quantidade em quilocalorias, em valor absoluto, envolvido na formação de 1 mol de metano dadas as seguintes variações de entalpia de combustão:
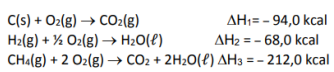
Assinale a alternativa correta.
Disciplina:
Química
A reação I e II representam reações de oxirredução que ocorrem em pilhas alcalinas.
I.2 MnO2(s) + H2O(ℓ) + 2 e⁻ → Mn2O3(s) + 2 OH⁻(aq)
II. Zn(s) + 2 OH- (aq) → ZnO(s) + H2O(ℓ) + 2 e⁻
As pilhas alcalinas começaram a ser produzidas no Brasil em 1978. A diferença básica entre essa pilha e a de Zn-C é que a primeira emprega célula eletroquímica com materiais ativos de maior grau de pureza. As pilhas alcalinas são mais resistentes a altas temperaturas, oferecem maior segurança contra vazamentos e duram de quatro a dez vezes mais que as Zn-C dependendo do uso. (https://www.scielo.br acesso em 16/04/2023)
Entre as vantagens dessa nova pilha está o fato de não ocorrer a formação de gases durante o processo redox, eliminando-se, portanto, os riscos de explosões. Sabendo-se que o potencial padrão de redução, E°, do zinco e do manganês, nos processos I e II, é -1,25 V e + 0,29 V, respectivamente, calcule a voltagem produzida pela pilha.
I.2 MnO2(s) + H2O(ℓ) + 2 e⁻ → Mn2O3(s) + 2 OH⁻(aq)
II. Zn(s) + 2 OH- (aq) → ZnO(s) + H2O(ℓ) + 2 e⁻
As pilhas alcalinas começaram a ser produzidas no Brasil em 1978. A diferença básica entre essa pilha e a de Zn-C é que a primeira emprega célula eletroquímica com materiais ativos de maior grau de pureza. As pilhas alcalinas são mais resistentes a altas temperaturas, oferecem maior segurança contra vazamentos e duram de quatro a dez vezes mais que as Zn-C dependendo do uso. (https://www.scielo.br acesso em 16/04/2023)
Entre as vantagens dessa nova pilha está o fato de não ocorrer a formação de gases durante o processo redox, eliminando-se, portanto, os riscos de explosões. Sabendo-se que o potencial padrão de redução, E°, do zinco e do manganês, nos processos I e II, é -1,25 V e + 0,29 V, respectivamente, calcule a voltagem produzida pela pilha.
Disciplina:
Química
Ocorre uma reação química quando se junta ácido clorídrico concentrado a carbonato de cálcio que dá origem a uma solução aquosa de cloreto de cálcio e à libertação de um gás (dióxido de carbono). A reação entre o ácido clorídrico concentrado e o carbonato de cálcio pode ser traduzida pela seguinte equação química:
2HCl (aq) + CaCO3 (s) → CaCl2 (aq) + H2O (l) + CO2 (g)
Pensando nas condições normais de temperatura e pressão (CNTP), vamos calcular a massa de água, em gramas, e o volume de gás carbônico, que pode se formar a partir de 80g de carbonato de cálcio. Dados as massas atômicas de Ca= 40; C = 12; O=16. Assinale a alternativa que apresenta os valores encontrados.
2HCl (aq) + CaCO3 (s) → CaCl2 (aq) + H2O (l) + CO2 (g)
Pensando nas condições normais de temperatura e pressão (CNTP), vamos calcular a massa de água, em gramas, e o volume de gás carbônico, que pode se formar a partir de 80g de carbonato de cálcio. Dados as massas atômicas de Ca= 40; C = 12; O=16. Assinale a alternativa que apresenta os valores encontrados.
Disciplina:
Química
Ao misturarmos o volume de um copo de álcool anidro com o volume correspondente a quatro copos de gasolina, portanto, a mistura em porcentagem aproximada, em volume de álcool será ______. Assinale a alternativa que preencha corretamente a lacuna.
Disciplina:
Química
Em relação às ligações químicas e aos compostos orgânicos (funções orgânicas) analise as afirmativas abaixo.
I. As ligações químicas nos compostos orgânicos podem ser do tipo s ou p . A ligação s é formada pela interação de dois orbitais atômicos, segundo o eixo que une os dois átomos, ao passo que na ligação p, a interação dos orbitais atômicos se faz segundo o plano que contém o eixo da ligação.
II Neste composto orgânico podemos encontrar 2 ligações s e 6 ligações p.
III. Neste composto orgânico podemos encontrar 3 ligações s e 6 ligações p.
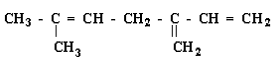
Estão corretas as afirmativas:
I. As ligações químicas nos compostos orgânicos podem ser do tipo s ou p . A ligação s é formada pela interação de dois orbitais atômicos, segundo o eixo que une os dois átomos, ao passo que na ligação p, a interação dos orbitais atômicos se faz segundo o plano que contém o eixo da ligação.
II Neste composto orgânico podemos encontrar 2 ligações s e 6 ligações p.
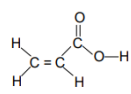
III. Neste composto orgânico podemos encontrar 3 ligações s e 6 ligações p.
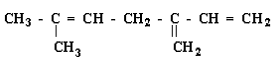
Estão corretas as afirmativas: