Questões de Concurso
Filtrar
212 Questões de concurso encontradas
Página 13 de 43
Questões por página:
Questões por página:
Em um recipiente de 104mL foram colocados 0,020 mmol de pentacloreto de fósforo submetido a uma temperatura elevada, e então este composto converteu-se ao cloreto de fósforo trivalente após a decomposição térmica. O sistema em questão é reversível e tende ao equilíbrio químico. Atingida esta condição, verificou-se que a concentração do gás formado foi de 0,7 mol/L. Assim sendo, a constante de equilíbrio calculada para este processo será, aproximadamente
Um experimento muito usado nas demonstrações de equilíbrio dinâmico é a mistura de NO2 e N2O4 . Este último é um gás que se liquefaz a 21ºC e congela a -11ºC, dímero do primeiro, o monômero. Considere a reação do monômero (2 mol/L) resultando no dímero (1 mol/L) em condições normais de temperatura e pressão e assinale a alternativa que indica o valor correto de Kc nessas condições.
mostrar texto associado
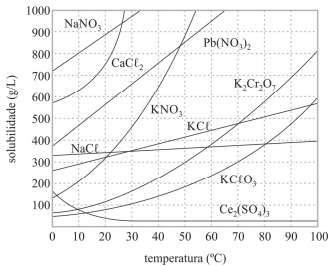
Com base no gráfico precedente, que apresenta as solubilidades em água de algumas substâncias, e considerando que as massas molares do NaNO3 e do KCl valham, respectivamente,85,00 g/mol e 74,6 g/mol, julgue o próximo item.
Em solução supersaturada, a concentração de soluto é superior à sua solubilidade a uma dada temperatura; mesmo assim, esse soluto permanece dissolvido após aquecimento e lento resfriamento do sistema.
Em solução supersaturada, a concentração de soluto é superior à sua solubilidade a uma dada temperatura; mesmo assim, esse soluto permanece dissolvido após aquecimento e lento resfriamento do sistema.
mostrar texto associado
Com base no gráfico precedente, que apresenta as solubilidades em água de algumas substâncias, e considerando que as massas molares do NaNO3 e do KCl valham, respectivamente,85,00 g/mol e 74,6 g/mol, julgue o próximo item.
A 50 °C, uma solução de 100 mL que contém 80 g de KNO3 é classificada como insaturada.
A 50 °C, uma solução de 100 mL que contém 80 g de KNO3 é classificada como insaturada.
mostrar texto associado
Com base no gráfico precedente, que apresenta as solubilidades em água de algumas substâncias, e considerando que as massas molares do NaNO3 e do KCl valham, respectivamente,85,00 g/mol e 74,6 g/mol, julgue o próximo item.
Uma solução de cloreto de potássio a 10 °C possui concentração em quantidade de matéria superior a 4,2 mol/L.
Uma solução de cloreto de potássio a 10 °C possui concentração em quantidade de matéria superior a 4,2 mol/L.