Questões de Concurso
Filtrar
206 Questões de concurso encontradas
Página 4 de 42
Questões por página:
Questões por página:
Considerando que o ácido glicólico, C2H4O3, é um ácido carboxílico com apenas um hidrogênio ionizável e grau de ionização menor que 5,0%, cujo Ka = 1,47 x 10−4, o pH de uma solução contendo 0,05 mol L−1 de ácido glicólico é:
Dados: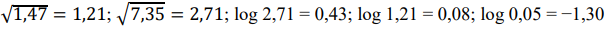
Dados:
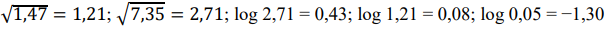
Um técnico de laboratório preparou uma solução somente com ácido acético, em uma concentração de 0,5 mol/ L. Considerando que Ka (25ºC) = 1,8 ⋅ 10-5, qual é a concentração de H3O+, em mol/L, nessa solução em equilíbrio?