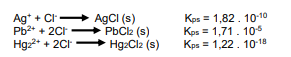Questões de Concurso
Filtrar
206 Questões de concurso encontradas
Página 6 de 42
Questões por página:
Questões por página:
Diversos processos de análises de materiais químicos ou de desenvolvimento de novos produtos envolvem diferentes tipos de equilíbrios químicos, os quais poderão envolver aspectos termodinâmicos, para os quais o/a analista deverá estar apto/a para lidar com eles. No equilíbrio químico, ou seja, em condições de temperatura e de pressão constantes, as atividades de todas as substâncias envolvidas nesse processo possuem um “valor de equilíbrio”, nomeado constante de equilíbrio, que é representada pela letra K.
Sobre o equilíbrio químico, dadas as afirmativas,
I. Para reações exotérmicas, quando a temperatura aumenta a composição da mistura em equilíbrio, há deslocamento em favor dos produtos e o oposto ocorre para as reações endotérmicas.
II. A energia livre de Gibbs pode ser relacionada à constante K, em que o ∆G t° (valor da energia de Gibbs no equilíbrio) é positivo; então, ln K (logaritmo natural da constante de equilíbrio) deverá ser negativo e, portanto, K < 1, indicando que os reagentes estão sendo favorecidos no equilíbrio químico.
III. A energia livre de Gibbs pode ser relacionada à constante K, em que o ∆G t° (valor da energia de Gibbs no equilíbrio) é negativo; então, ln K (logaritmo natural da constante de equilíbrio) deverá ser negativo e, portanto, K > 1, indicando que os produtos estão sendo favorecidos no equilíbrio químico.
verifica-se que está/ão correta/s
Sobre o equilíbrio químico, dadas as afirmativas,
I. Para reações exotérmicas, quando a temperatura aumenta a composição da mistura em equilíbrio, há deslocamento em favor dos produtos e o oposto ocorre para as reações endotérmicas.
II. A energia livre de Gibbs pode ser relacionada à constante K, em que o ∆G t° (valor da energia de Gibbs no equilíbrio) é positivo; então, ln K (logaritmo natural da constante de equilíbrio) deverá ser negativo e, portanto, K < 1, indicando que os reagentes estão sendo favorecidos no equilíbrio químico.
III. A energia livre de Gibbs pode ser relacionada à constante K, em que o ∆G t° (valor da energia de Gibbs no equilíbrio) é negativo; então, ln K (logaritmo natural da constante de equilíbrio) deverá ser negativo e, portanto, K > 1, indicando que os produtos estão sendo favorecidos no equilíbrio químico.
verifica-se que está/ão correta/s
Assinale a opção que apresenta o pH de uma solução de um ácido monoprótico (Ka = 2,0 x 10-6 ) com concentração de 2,0 M. Dado: log10 2 ≈ 0,3.
Concurso:
SAE de Catalão - GO
Disciplina:
Química
O pH é um parâmetro importante a ser considerado no processo de tratamento de água e de efluentes. Na agricultura, o uso de cal hidratada (Ca(OH)2) no processo de calagem e de fertilizantes como o nitrato de amônio (NH4NO3), podem afetar o pH de água de rios.
Sobre a alteração no pH acarretada por cada uma das substâncias citadas, assinale a única alternativa correta.
Concurso:
Prefeitura de Pouso Alegre - MG
Disciplina:
Química
Analise as alternativas a seguir.
I. Copo com álcool hidratado.
II. Copo com água e gelo.
III. Copo de água com gás.
O sistema heterogêneo com duas fases é observado apenas em:
Concurso:
Prefeitura de Santos
Disciplina:
Química
mostrar texto associado
O precipitado branco da questão anterior (que havia sido completamente precipitado com HCl diluído), foi recolhido após filtração, recebeu mais 10 ml de água destilada e foi aquecido em banho-maria até a temperatura de ebulição da água, mantido assim por cerca de 5 minutos. Esse processo de aquecimento dissolveu todo material que estava precipitado. Isso indicou que apenas um dos 3 cloretos estava presente no sal branco que havia precipitado, já que dois deles são tão insolúveis que não se redissolveriam com o aquecimento na solução aquosa, sem que ocorressem mudanças no pH da solução. Com base nas informações fornecidas, assinale a alternativa que apresenta qual dos 3 cátions estava presente na solução amostra: Ag+, Pb2+ ou Hg2 2+ .