Filtrar
332 Questões de concurso encontradas
Página 1 de 67
Questões por página:
Questões por página:
Uma determinada substância tem seu calor específico governado pela seguinte função c(T) = 2 + 3T² + 0,4T³, sendo T em °C e c em cal/g.K. Calcule a energia necessária para aumentar a temperatura de um corpo de massa igual a 30g de 3 °C para 30 °C.
Um recipiente de alumínio com coeficiente de dilatação linear igual a 23 x 10-6 °C-1 possui um volume de 100 cm³ e está preenchido de um líquido a 22 °C. Após o conjunto, recipiente e líquido, atingirem a temperatura de 28°C uma parte do líquido é derramada. Sendo o coeficiente de dilatação volumétrica do líquido igual a 5,1 x 10-4 °C-1, calcule o volume do líquido derramado.
Um cilindro maciço, de raio igual a 5 cm, a altura igual a 15,0 cm e emissividade 0,75, a uma temperatura de 27 °C, está suspenso em um ambiente de temperatura igual a 60 °C. Calcule, aproximadamente, a taxa líquida de transferência de radiação térmica.
Após a variação de temperatura em 100°C de um cilindro metálico, o seu comprimento aumentou em 0,32%. Calcule o módulo da variação percentual da massa específica.
mostrar texto associado
Uma certa massa de gás ideal passa pelo processo termodinâmico ilustrado na figura ao lado, que apresenta um diagrama P x V (pressão em função do volume).
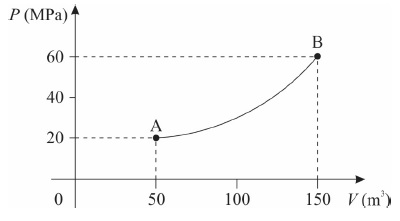
Considerando que a temperatura do gás no ponto A vale TA = 50 K, assinale a alternativa que apresenta corretamente a temperatura TB do gás no ponto B.

Considerando que a temperatura do gás no ponto A vale TA = 50 K, assinale a alternativa que apresenta corretamente a temperatura TB do gás no ponto B.