Filtrar
10 Questões de concurso encontradas
Página 1 de 2
Questões por página:
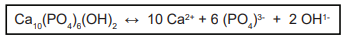
A solução aquosa capaz de evitar a desmineralização dos dentes é:
Ni2+(aq) + 3 en (aq) ↔ Ni(en)32+ (aq)
en = 1,2 etilenodiamina
Ni2+ (aq) + 6 NH3 (aq) ↔ Ni(NH3 )6 2+ (aq)
Uma das explicações para essa constatação experimental está relacionada ao:
Um método simples de se reduzir a concentração de íons prata (Ag+ ) livres em solução aquosa é através da adição de amônia (NH3 ) a mesma, resultando na formação do complexo Ag(NH3 )2 +, cuja constante de formação (kf ) é igual a 1,7 x 107, a 25ºC. Indique qual a concentração de Ag+ presente em uma solução em equilíbrio quando amônia concentrada é adicionada a solução de AgNO3 0,010 mol L-1 para fornecer uma concentração de amônia no equilíbrio de 0,20 mol L-1 .
Desprezar a variação de volume causada pela adição de NH3 .
Como acontece com todas as ionizações, a água também se ioniza em um processo reversível até atingir um estado de equilíbrio, denominado equilíbrio iônico da água. A respeito dos conceitos do produto iônico da água e de pH e pOH, julgue o item a seguir. Dado: Kw = 1,0x10-14.
A expressão matemática do produto iônico da água é: Kw = [H+] / [OH- ].