Questões de Concurso
Filtrar
49 Questões de concurso encontradas
Página 8 de 10
Questões por página:
Um estudante misturou 50 mL de solução aquosa de ácido sulfúrico 0,10 mol/L com 50 mL de solução aquosa de hidróxido de sódio 0,40 mol/L e introduziu algumas gotas de fenolftaleina. O processo pode ser representado pela equação não balanceada:
H2SO4(aq) + NaOH(aq) → Na2SO4(aq) + H2O(l)
Ao término da reação, pode-se concluir acertadamente queConsidere as duas soluções aquosas ácidas apresentadas a seguir:
I. Ácido sulfúrico (H2SO4), um ácido forte (α = 100%),0,1 mol/L.
II. Ácido acético (CH3COOH), um ácido fraco (α = 10%),0,1 mol/L.
O pOH do ácido sulfúrico e o pH do ácido acético são respectivamente
A solubilidade dos sulfetos depende fortemente do pH do meio. Por esse motivo, muitas vezes a precipitação desses compostos é realizada em meio tamponado. Considerando que pOH = -log [OH- ] e pKb = -log Kb, julgue o seguinte item.
Uma solução-tampão constituída por NH4Cℓ 0,040 mol/L e NH3 (aq) 0,030 mol/L apresenta pOH superior ao pKb da NH3.
Tendo a figura e as informações precedentes como referência, julgue o item subsequente.
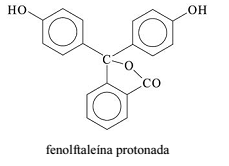
Considerando que a fenolftaleína seja incolor em pH reduzido e rosa em pH elevado, infere-se que a forma protonada da fenolftaleína é a que apresenta coloração rosa.