Questões de Concurso
Filtrar
430 Questões de concurso encontradas
Página 6 de 86
Questões por página:
Questões por página:
mostrar texto associado
Avogadro (1776-1856) estimou que o diâmetro de um átomo é em torno de 10-10 m. Um século mais tarde, Ernest Rutherford (1871-1937) estimou que os núcleos atômicos possuem diâmetro de cerca de 10–14m.
A diferença entre os diâmetros foi explicada pela presença de prótons e nêutrons no núcleo muito denso e pela disposição de elétrons em camadas na eletrosfera, num modelo atômico planetário.
A esse respeito, analise as afirmativas a seguir.
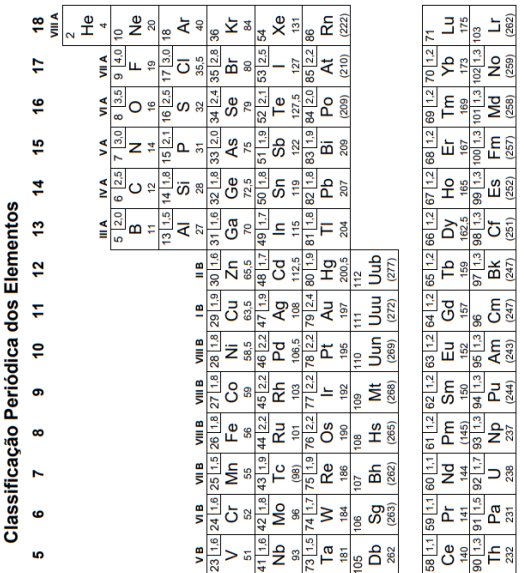
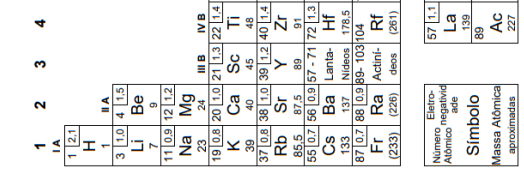
I. O raio atômico do estrôncio é igual ao raio atômico da prata, pois ambos átomos possuem o mesmo número de camadas eletrônicas.
II. O raio atômico do cálcio é maior do que o raio atômico do bário, pois o cálcio apresenta maior número de camadas eletrônicas.
III. O raio atômico do potássio é maior do que o raio atômico do zinco, pois o potássio tem menor carga nuclear.
Está correto o que se afirma em
A diferença entre os diâmetros foi explicada pela presença de prótons e nêutrons no núcleo muito denso e pela disposição de elétrons em camadas na eletrosfera, num modelo atômico planetário.
A esse respeito, analise as afirmativas a seguir.
I. O raio atômico do estrôncio é igual ao raio atômico da prata, pois ambos átomos possuem o mesmo número de camadas eletrônicas.
II. O raio atômico do cálcio é maior do que o raio atômico do bário, pois o cálcio apresenta maior número de camadas eletrônicas.
III. O raio atômico do potássio é maior do que o raio atômico do zinco, pois o potássio tem menor carga nuclear.
Está correto o que se afirma em
mostrar texto associado
O efeito fotoelétrico é um fenômeno de origem quântica que consiste na emissão de elétrons por algum material que é iluminado por radiações eletromagnéticas de frequências específicas. Os elétrons emitidos por esses materiais são chamados de fotoelétrons.
Considere os átomos sódio (Na), potássio (K), ferro (Fe), césio (Cs) e iodo (I).
Nesse conjunto, o átomo que necessita de radiação eletromagnética de menor frequência para a emissão de fotoelétrons é
Considere os átomos sódio (Na), potássio (K), ferro (Fe), césio (Cs) e iodo (I).
Nesse conjunto, o átomo que necessita de radiação eletromagnética de menor frequência para a emissão de fotoelétrons é
mostrar texto associado
O carbono possui 3 isótopos naturais: 6C12, 6C13 e 6C14. As abundâncias dos isótopos 6C12 e 6C13 são, respectivamente,98,9% e 1,1%, restando apenas traços do 6C14.
Sobre os átomos 6C12, 6C13 e 6C14, é correto afirmar que eles possuem
Sobre os átomos 6C12, 6C13 e 6C14, é correto afirmar que eles possuem
mostrar texto associado
O escândio é um elemento químico de símbolo Sc que apresenta número atômico igual a 21. É sólido a 25ºC, metálico, macio, de cor branco-prateada.
A configuração eletrônica do escândio, no estado fundamental, é:
A configuração eletrônica do escândio, no estado fundamental, é:
mostrar texto associado
O radônio é classificado como um gás nobre, sendo que, entre os elementos desse grupo até hoje conhecidos, o radônio é o que apresenta menor eletronegatividade.