Questões de Concurso
Filtrar
3.192 Questões de concurso encontradas
Página 309 de 639
Questões por página:
CAMPOS, B. Instituto Geral de Perícias de Santa Catarina. Disponível em: <https://www.sc.gov.br/noticias/temas/defesa civil-e-bombeiros/perito-do-igp-explica-semelhancas-entreexplosao -em-beirute-e-incidente-em-sao-francisco-do-sul>. Acesso em: 20 ago.2020 (Adaptação).
Considerando que 20 toneladas do fertilizante com 65%m/m em nitrato de amônio foram expostas ao acidente e todo o nitrato foi queimado, qual é a massa mais próxima, em toneladas, de nitrogênio, detonada na explosão?
O sulfito de sódio (Na2SO3 ) é um sal inorgânico muito utilizado como conservante de alimentos e na manufatura de papel. Um dos processos de produção do sulfito de sódio pode ser obtido mediante a seguinte equação na condição de equilíbrio químico.
Na2O(s) + SO2(g) ⇋ Na2SO3(s) ∆H < 0
Considerando que para a reação de produção em um processo industrial é desejável que se produza mais sulfito de sódio partindo de um sistema em equilíbrio, qual fator é adequado para tal processo?
Em um experimento de química, um estudante colocou em um recipiente 500 mL de uma solução aquosa de hidróxido de sódio (NaOH) em uma chapa de aquecimento. O pOH da solução antes do aquecimento era igual a 2. Após um tempo, considerando que se evaporou apenas água, o pOH da solução se reduziu à metade.
Nessas condições, é correto afirmar que o volume, em mililitros, da solução que permaneceu no recipiente ao fim do experimento é igual a
Em condições ideais, pequenas quantidades de gás cloro podem ser geradas em laboratório pela reação do óxido de manganês (MnO2 ) com ácido clorídrico (HCl), conforme a equação química a seguir não balanceada.
HCl(aq) + MnO2 (s) → H2O(L) + MnCl2(s) + Cl2(g)
A partir dessas informações, quantas moléculas de gás cloro, aproximadamente, podem ser produzidas quando 10 g de óxido de manganês com grau de pureza de 87% são colocados para reagir completamente com excesso de ácido clorídrico?
Dado: Número de Avogadro (N) = 6 x 1023
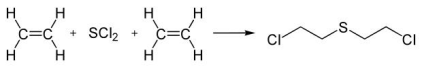
Sobre a equação de produção do gás mostarda, foram feitas a seguintes afirmações:
I. O eteno é um composto isomérico trans. II. O gás mostarda tem fórmula molecular C4H8SCl2 . III. A reação orgânica de produção do gás mostarda é de substituição.
São incorretas as afirmações