Questões de Concurso
Filtrar
3.317 Questões de concurso encontradas
Página 538 de 664
Questões por página:
Questões por página:
Concurso:
TRANSPETRO
Disciplina:
Química
A incerteza associada a um resultado analítico tem como origem os erros aleatórios de todas as etapas do processo. A correção de qualquer fonte de erro sistemático do processo se faz necessária para um cálculo de incerteza adequado.
Sobre os erros do processo analítico, pode-se afirmar que
Sobre os erros do processo analítico, pode-se afirmar que
Concurso:
TRANSPETRO
Disciplina:
Química
Várias fases sólidas são usadas para obter-se separação entre espécies químicas tirando vantagem de pequenas diferenças em alguma propriedade de duas ou mais espécies químicas. Dentre essas propriedades, NÃO se inclui
Concurso:
TRANSPETRO
Disciplina:
Química
A separação de íons em solução por meio de precipitação seletiva é uma prática muito importante em química analítica. A abordagem que NÃO pode ser usada para separação de íons em solução é a(o)
Concurso:
TRANSPETRO
Disciplina:
Química
Um técnico dispõe de dois frascos. Um contendo solução de KOH 0,5 mol L-1 e outro contendo solução de NaOH 1,5 mol L-1 . Ele transferiu 40 mL da solução de KOH e 60 mL da solução de NaOH para um cilindro graduado de 1,0 L, acrescentou água destilada até o traço de referência (1,0 L) e, em seguida, homogeneizou bem a mistura.
Com esses procedimentos, ele obteve uma solução final cuja concentração de OH- em quantidade de matéria (mol L-1 ) é
Com esses procedimentos, ele obteve uma solução final cuja concentração de OH- em quantidade de matéria (mol L-1 ) é
Concurso:
TRANSPETRO
Disciplina:
Química
Na temperatura ambiente, cloreto de sódio e sulfato de potássio são sais que, dissolvidos em água, liberam íons que não se hidrolisam. Acetato de potássio, bicarbonato de sódio e cloreto de amônio são sais que liberam íons quando dissolvidos em água; desses, há os que se hidrolisam e os que não se hidrolisam.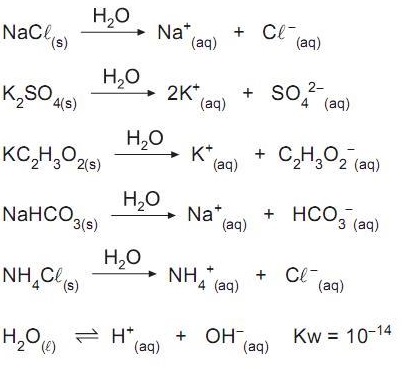
Considerando os íons dos sais que reagem com a água (hidrólise) e os que não reagem, afirma-se que a solução aquosa de