Questões de Concurso
Filtrar
38 Questões de concurso encontradas
Página 4 de 8
Questões por página:
Com os uniformes cobertos de barro, os militares bombeiros estavam por todos os lados no mar de lama e detritos que arrasou a cidade de Brumadinho devido ao acidente da barragem ocorrido no ano de 2019. A lama de rejeito provocou um rastro de destruição ao longo do Rio Paraopeba. Segundo especialistas, em toda a extensão percorrida, a água do rio não tinha condições para o consumo humano e animal. Dentre vários contaminantes, encontraram-se metais em altas concentrações como ferro, cobre, manganês e cromo.
Sobre os metais citados no texto, aquele que, quando o átomo se encontra ionizado no estado de oxidação +2 apresentará a configuração eletrônica 1s2 2s2 2p6 3s2 3p6 3d5 é o:
O modelo atômico de Bohr contribuiu muito para a implantação do modelo atual. Uma das contribuições foi a proposição de que os elétrons existem apenas em níveis de energia distintos e que são descritos pelos números quânticos. Dentro desse contexto, Bohr inseriu no vocabulário científico a ideia de estados fundamentais e excitados para descrever o comportamento dos elétrons nos átomos.
Considerando essas informações, assinale a alternativa que representa a configuração eletrônica em que o átomo se encontra no estado excitado.
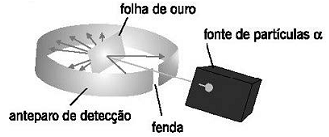
Disponível em:: <http://objetoseducacionais2.mec.gov.br/bitstream/handle/mec/12908/08_avaliacao.htm> . Acesso em: 11 jan.2016.
Com esse experimento, é possível concluir:
Moléculas de lítio não existem no estado líquido ou sólido, mas, sem dúvida, as moléculas diatômicas são encontradas no lítio gasoso. A energia de ligação do Li2 é 105 kJ/mol.
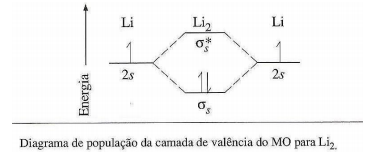
Sobre o diagrama de população da camada de valência do MO para Li2, analise as afirmativas a seguir.
I. A ordem de ligação é 1/2.
II. A configuração eletrônica de Li2 pode ser escrita como KK (σs)2 .
III. A energia de ligação do Li2 é menor do que H2 porque há uma blindagem do núcleo pela camada K completa de cada átomo.
Está(ão) correta(s) apenas a(s) afirmativa(s)
Para combater a classe de incêndios gerados por esses materiais, deve-se empregar um extintor de pó químico elaborado à base de cloreto de sódio (NaCl).
Considerando o texto acima e os múltiplos aspectos que ele suscita, julgue os itens a seguir, utilizando, caso necessário, a tabela periódica inserida no final deste caderno de provas.
A concepção de átomo proposta por Rutherford permite explicar a coloração da chama emitida no processo de combustão do bário.