Questões de Concurso
Filtrar
66 Questões de concurso encontradas
Página 5 de 14
Questões por página:
Corrente Elétrica 10 A
Tempo 30 min
Pressão 1,0 atm
Temperatura 273 K
Sabendo que, nessas condições, foram recolhidos 1,7 L de gás hidrogênio é possível prever que o rendimento do processo foi, aproximadamente, de
(Dado: Constante de Faraday = 96.500 s.A.mol-1)
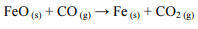
Caso essa reação seja realizada em etapas, as reações de cada etapa serão as seguintes, em que ∆Hn (n = 1,2 ou 3) representa a variação de entalpia da n-ésima etapa:
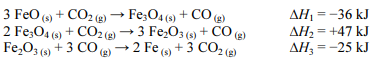
A partir da Lei de Hess, é possível calcular a variação de entalpia envolvida na primeira reação.
Nessa situação, considerando-se que MFe = 56 g/mol seja a massa molar do ferro, é correto concluir que a variação de entalpia envolvida na formação de 140 g de ferro metálico por meio da redução do óxido ferroso pelo monóxido de carbono é
Em meados do século XX, as pilhas alcalinas surgiram como uma alternativa muito mais eficiente energeticamente em comparação às pilhas tradicionais. Como mostra a seguinte figura, a pilha alcalina utiliza os mesmos eletrodos da tradicional, porém o seu eletrólito é uma solução aquosa de hidróxido de sódio concentrada (~30% em massa) contendo uma dada quantidade de óxido de zinco ― daí a denominação alcalina para essa pilha.
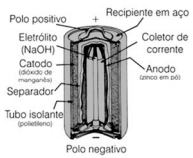
Internet:<http://qnesc.sbq.org.br> (com adaptações).
“Um banho de ouro consiste em mergulhar o metal-base em uma solução de sais de ouro e ligá-lo à corrente elétrica. Ao lado dele, mergulha-se uma barra de ouro ligada ao outro polo de corrente elétrica, que tem, nessas condições, a propriedade de transportar o ouro líquido e depositá-lo sobre a peça a ser dourada. O banho de ouro pode ser aplicado em diversos tipos de metal-base, como: prata, níquel, cobre e latão. Dependendo do tempo de duração da imersão da peça, essa camada poderá ser mais ou menos espessa. A boa douração tem espessura na ordem de 0,02 mm ou 20 mícrons.”
(Disponível em: https://agatarp.com.br/blog/2012/08/31/a-diferenca-entre-folheamento-e-o-banho-de-ouro/.)
Assinale a alternativa que corresponde ao número de mols de ouro utilizado em uma eletrodeposição de Au+ que durou 7 minutos e utilizou 4,6 A.
(Dados: massa molar do Au = 197g; 1F = 96500C; 1A = 1C/s.)