Questões de Concurso
Filtrar
133 Questões de concurso encontradas
Página 9 de 27
Questões por página:
Questões por página:
Concurso:
CONAB
Disciplina:
Engenharia Química e Química Industrial
Relacione CORRETAMENTE as técnicas de análise de risco com suas características, numerando a Coluna II de acordo com a Coluna I.
COLUNA I
1. AMFE. 2. HAZOP. 3. AAF.
COLUNA II
(__)Identifica riscos e desvios de parâmetros de processos.
(__)É dedutiva e utiliza um evento topo e constrói níveis subsequentes identificando falhas.
(__)Identifica os modos de falhas dos componentes de um sistema e seus efeitos.
A sequência CORRETA da correlação entre as colunas é:
COLUNA I
1. AMFE. 2. HAZOP. 3. AAF.
COLUNA II
(__)Identifica riscos e desvios de parâmetros de processos.
(__)É dedutiva e utiliza um evento topo e constrói níveis subsequentes identificando falhas.
(__)Identifica os modos de falhas dos componentes de um sistema e seus efeitos.
A sequência CORRETA da correlação entre as colunas é:
Concurso:
Prefeitura de Santos
Disciplina:
Engenharia Química e Química Industrial
O gesso é um material aglomerante, obtido a partir da Gipsita, mineral abundante em terrenos cretáceos no Brasil, como o polo gesseiro do Araripe, estado de Pernambuco. Seu principal componente é o Sulfato de Cálcio di-hidratado. Por meio de calcinação, parte da água de hidratação é retirada e o mineral é moído para formar um pó, usado na construção civil e na medicina, entre muitas outras aplicações. Quando se reidrata o Sulfato de Cálcio hemi-hidratado, com cerca de um terço de seu peso em água, ele volta ao seu estado di-hidratado. Nesse processo, o gesso endurece em alguns minutos, em uma reação perceptivelmente exotérmica, vista abaixo:
CaSO4 . ½ H2O (s) + 3/2 H2O (liq) ➞ CaSO4 .2 H2O (s) + Energia (Calor)
Analisando a variação de entalpia dessa reação:

Um paciente, que teve a perna engessada para imobilização ortopédica, se queixou que o gesso esquentou muito enquanto endurecia. Pode-se estimar a temperatura máxima da peça de gesso assim que se endurece, com base nos dados de entalpia da reação acima, fazendo as seguintes considerações:
- A temperatura ambiente na sala ortopédica ficou estável em 21 °C, não se alterando enquanto o gesso foi aplicado e endureceu;
- A pressão não variou ao longo do processo de endurecimento do gesso e os valores de entalpia de cada substância não são dependentes da temperatura;
- Todo o calor liberado pela reação seria expresso no aumento de temperatura da peça de gesso
([ΔHoReação] = ΔHoAquecimento do Gesso).
Assim, calculando com base na equação de Kirchhoff:
n . [ΔHoReação] = n . Cp . ΔT
Onde:
n = Número de moles Cp = Capacidade Calorífica do Gesso = 186,2 Joules.K-1.mol-1 ΔT = Variação da Temperatura da peça de Gesso (Temperatura final ºK – Temperatura Inicial do Gesso ºK)
Dada a equação de conversão entre °K (kelvin) em °C (celsius):
°C = °K - 273,15
Depois de aplicar o cálculo, considerando que toda a energia térmica da reação fosse acumulada no gesso, com relação à temperatura do gesso, é correto afirmar que
CaSO4 . ½ H2O (s) + 3/2 H2O (liq) ➞ CaSO4 .2 H2O (s) + Energia (Calor)
Analisando a variação de entalpia dessa reação:

Um paciente, que teve a perna engessada para imobilização ortopédica, se queixou que o gesso esquentou muito enquanto endurecia. Pode-se estimar a temperatura máxima da peça de gesso assim que se endurece, com base nos dados de entalpia da reação acima, fazendo as seguintes considerações:
- A temperatura ambiente na sala ortopédica ficou estável em 21 °C, não se alterando enquanto o gesso foi aplicado e endureceu;
- A pressão não variou ao longo do processo de endurecimento do gesso e os valores de entalpia de cada substância não são dependentes da temperatura;
- Todo o calor liberado pela reação seria expresso no aumento de temperatura da peça de gesso
([ΔHoReação] = ΔHoAquecimento do Gesso).
Assim, calculando com base na equação de Kirchhoff:
n . [ΔHoReação] = n . Cp . ΔT
Onde:
n = Número de moles Cp = Capacidade Calorífica do Gesso = 186,2 Joules.K-1.mol-1 ΔT = Variação da Temperatura da peça de Gesso (Temperatura final ºK – Temperatura Inicial do Gesso ºK)
Dada a equação de conversão entre °K (kelvin) em °C (celsius):
°C = °K - 273,15
Depois de aplicar o cálculo, considerando que toda a energia térmica da reação fosse acumulada no gesso, com relação à temperatura do gesso, é correto afirmar que
Concurso:
Prefeitura de Santos
Disciplina:
Engenharia Química e Química Industrial
A queima de combustíveis à base de Carbono, na presença de Oxigênio atmosférico, foi talvez a primeira tecnologia da engenharia química desenvolvida pelo ser humano. Quando dominamos o fogo, milênios antes de entendermos os princípios científicos envolvidos, aprendemos a reproduzir comportamentos empíricos e a contornar as dificuldades que apareciam, nos forçando a ser uma espécie cada vez mais criativa. Seguramente não foram poucos os dias de vento e chuva, onde os ancestrais humanos tiveram de usar musgo, cera das cascas de frutas e óleo de folhas de coníferas para aproveitar as chispas do novo conhecimento. Muito tempo se passou, a chama do conhecimento cresceu ainda mais e a humanidade decidiu explorar o espaço. Novamente, se deparou com dificuldades impensadas até então. Agora precisamos queimar metais (para obter maiores quantidades de energia) e levantar foguetes até superar a atmosfera terrestre. Exatamente lá onde não temos o oxigênio nos esperando com nossa fagulha de atrevimento. Mas encontramos soluções, como sempre fazemos.
Os poderosos combustíveis sólidos foram adotados inicialmente pela NASA em seus lançamentos e agora também sendo usados pelas agências privadas que prestam serviços aos governos, levando carga e passageiros para suas missões fora do planeta. As reações a seguir, representam as duas principais reações de oxirredução envolvidas na queima dos combustíveis sólidos dos foguetes:
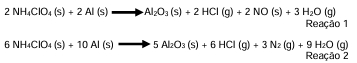
Analisando ambas as reações combinadas, fica evidente que o alumínio passa do estado de oxidação (zero) para (3+), enquanto o cloro passa de (+7) para (-1). Assim, pode-se concluir nessa análise que o estado de oxidação de nitrogênio vai de
Os poderosos combustíveis sólidos foram adotados inicialmente pela NASA em seus lançamentos e agora também sendo usados pelas agências privadas que prestam serviços aos governos, levando carga e passageiros para suas missões fora do planeta. As reações a seguir, representam as duas principais reações de oxirredução envolvidas na queima dos combustíveis sólidos dos foguetes:
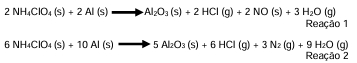
Analisando ambas as reações combinadas, fica evidente que o alumínio passa do estado de oxidação (zero) para (3+), enquanto o cloro passa de (+7) para (-1). Assim, pode-se concluir nessa análise que o estado de oxidação de nitrogênio vai de
Concurso:
Prefeitura de Santos
Disciplina:
Engenharia Química e Química Industrial
A reação de queima do alumínio na oxirredução que envolve o poderoso oxidante perclorato de amônio e forma tri-óxido-de-di-alumínio (responsável pelo interminável rastro branco deixado nos céus durante os lançamentos), ácido clorídrico, gás nitrogênio, óxido nitroso, e água. Em seu balanço de massa, vemos que 69,6% do peso é referente ao oxidante, enquanto o combustível (alumínio metálico) corresponde a 16%. Imagina-se que para atingir o ponto de queima de metais, temos de superar uma importante energia de ativação. Por conta disso, temos a participação de um catalizador à base de óxido de ferro (0,4% do peso da mistura). Fundamental nesse sistema, temos ainda 12,04% de um polímero aglutinante (para manter os ingredientes posicionados e garantir a continuidade da combustão). Afinal temos uma força explosiva tentando separar toda a mistura e não contamos com a convergente força da gravidade, que temos sempre quando estamos com os pés na terra. O complemento é dado por 1,96% do peso total em um agente à base de resina epóxi para assegurar a cura do polímero aglutinante. Sem contar que esse tipo de combustível, depois de aceso no foguete, não pode ser parado. Realmente, avançamos muito nos processos, ingredientes e tecnologias da combustão desde que começamos a queimar galhos secos de árvores, incendiados com uma faísca vinda de duas pedras se chocando. Apesar dessa incrível jornada tecnológica, os processos de combustão seguem todos os princípios simples e semelhantes. Sobre o assunto, assinale a alternativa mais adequada para resumir a combustão.
Concurso:
Prefeitura de Santos
Disciplina:
Engenharia Química e Química Industrial
A absorbância de uma amostra foi medida em condições padronizadas a partir de uma fonte de luz conhecida e colimada em determinado comprimento de onda, caminho ótico conhecido em uma cubeta de dimensões padronizadas e um indicador eletrônico da intensidade da luz absorvida pela amostra. Sabendo que o valor da absorbância medida é proporcional à concentração da substância amostrada na cubeta de acordo com a equação de Lambert–Beer:
A = εbc
Onde:
A é a absorbância da amostra; ε é a absortividade molar da substância analisada; b é o comprimento do caminho seguido pela luz, convencionado em medida unitária (cubeta quadrada de 1 cm por 1 cm); c é a concentração da espécie absorvente.
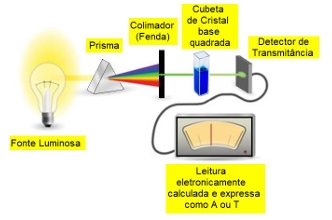
Comparando-se 3 amostras da mesma substância entre si, chega-se a 3 leituras diferentes de Absorbância, medidas sempre no mesmo comprimento de onda de 540 nm:
Amostra 1 ………… A1 = 2,0
Amostra 2 ………… A2 = 4,0
Amostra 3 ..……….. A3 = 1,0
A partir desses resultados, é correto afirmar que a amostra
A = εbc
Onde:
A é a absorbância da amostra; ε é a absortividade molar da substância analisada; b é o comprimento do caminho seguido pela luz, convencionado em medida unitária (cubeta quadrada de 1 cm por 1 cm); c é a concentração da espécie absorvente.

Comparando-se 3 amostras da mesma substância entre si, chega-se a 3 leituras diferentes de Absorbância, medidas sempre no mesmo comprimento de onda de 540 nm:
Amostra 1 ………… A1 = 2,0
Amostra 2 ………… A2 = 4,0
Amostra 3 ..……….. A3 = 1,0
A partir desses resultados, é correto afirmar que a amostra