Questões de Concurso
Filtrar
49 Questões de concurso encontradas
Página 4 de 10
Questões por página:
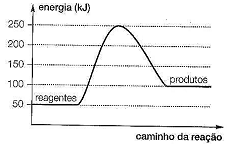
Considerando o gráfico anterior, referente ao diagrama energético de uma reação química, qual o valor da energia de ativação e o ΔH da reação respectivamente?
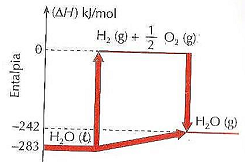
A partir do diagrama de entalpia, marque V para as afirmativas verdadeiras e F para as falsas.
( ) A quantidade de calor envolvido na decomposição de 126 g de H2O(l) → H2(g) + ½ O2(g) é 1.981 kJ/mol.
( ) H2O(l) → H2O(g) ΔH = –41 kJ/mol.
( ) H2(g) + ½ O2(g)→ H2O(g) ΔH = +242 kJ/mol.
A sequência está correta em
Com os problemas de natureza sanitária causados pela pandemia gerada pela Covid-19, o Corpo de Bombeiros Militar de Minas Gerais tem realizado ações que visam orientar a população quanto ao uso do álcool em gel 70 ºINPM (grau INPM – Instituto Nacional de Pesos e Medidas) ou (70% p/p). O fato é que o álcool em gel se tornou um poderoso combatente no processo de higienização das mãos e proteção contra o novo coronavírus. Entretanto, não se deve nos esquecer de que, além de um eficiente desinfetante, o álcool é uma substância inflamável. Ele também tem sido a causa de muitos acidentes domésticos devido ao seu uso inadequado.
A equação a seguir representa a combustão de um mol de molécula do etanol:
CH3CH2OH + 3O2 → 2 CO2 + 3 H2O
ΔH° = - 1373kJ
O etanol é o tipo de álcool utilizado no álcool em gel. Se considerar apenas o álcool 70 ºINPM como constituinte do álcool em gel e que 460 g desse composto foram completamente queimados, qual a energia, em kJ, mais próxima liberada nesse processo?
As equações químicas a seguir representam o processo de síntese dos óxidos de bário e alumínio e suas respectivas entalpias de transformação.
2Ba(s) + O2 (g) → 2 BaO(s) ΔHº = –1.107 kJ
2Al(s) + 3/2O2 (g) → Al2 O3 (s) ΔHº = –1.676 kJ
O metal bário é produzido pela reação do metal alumínio com óxido de bário. A partir dessas informações, a variação da entalpia para a reação de produção do metal bário é igual a:
Um depósito contendo cinco tipos de combustíveis pegou fogo. Após o incêndio surgiram discussões à cerca dos que eram guardados pressurizados, por se tratarem de gases na temperatura ambiente e a 1 atm.
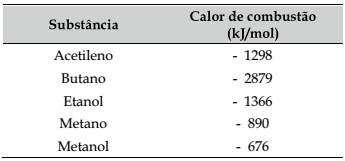
Considere os dados fornecidos nessa tabela, levando em conta apenas o alvo das discussões descritas.
Logo, o combustível que vai liberar maior quantidade de energia, em kj, por unidade de massa queimada, é o