Questões de Concurso
Filtrar
3.317 Questões de concurso encontradas
Página 245 de 664
Questões por página:
Questões por página:
Disciplina:
Química
A seguinte figura mostra os estados físicos da matéria e as mudanças de estados I, II, III e IV.
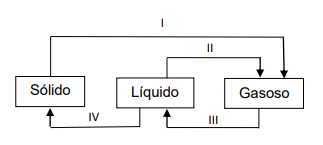
Assinale a opção que apresenta corretamente todas as mudanças de estados.

Assinale a opção que apresenta corretamente todas as mudanças de estados.
Disciplina:
Química
Na natureza, a água passa de um estado físico para outro constantemente e está sempre mudando de lugar. Esse movimento é chamado de ciclo da água. A respeito desse ciclo, é correto afirmar que
Disciplina:
Química
O ácido sulfúrico é um ácido poliprótico que possui duas deprotonação. A primeira deprotonação é _____ _, já que é um ácido ______. A segunda deprotonação possui uma constante Ka2=0,012.
Essa característica faz que uma solução de ácido sulfúrico de concentração 0,01 mol l-1 tenha um pH de ______ .
Assinale a alternativa que preench a correta e respectivamente as lacunas.
Essa característica faz que uma solução de ácido sulfúrico de concentração 0,01 mol l-1 tenha um pH de ______ .
Assinale a alternativa que preench a correta e respectivamente as lacunas.
Disciplina:
Química
Uma das condições mais interessantes das soluções é a chamada elevação do ponto de ebulição ou o abaixamento no ponto de congelamento. Diante do exposto, analise as asserções a seguir.
I. Em países onde o inverno é rigoroso, usa -se o NaCl nas estradas para abaixar o ponto de congelamento da água e retardar a formação do gelo. II. Na presença de um soluto, a temperatura de ebulição da água sobe (pouco) para 100,05º C na presença de 0,1M de sacarose. III. A água do mar possui uma temperatura de congelamento maior de 0º C devido à mistura de muitos sais dissolvidos.
Estão corretas as asserções :
I. Em países onde o inverno é rigoroso, usa -se o NaCl nas estradas para abaixar o ponto de congelamento da água e retardar a formação do gelo. II. Na presença de um soluto, a temperatura de ebulição da água sobe (pouco) para 100,05º C na presença de 0,1M de sacarose. III. A água do mar possui uma temperatura de congelamento maior de 0º C devido à mistura de muitos sais dissolvidos.
Estão corretas as asserções :
Disciplina:
Química
Considerando que os átomos de oxigênio possuem os isótopos 16O, 17O e 18O . O carbono possui os isótopos 12C, 13C e 14C
I. São possíveis 9 combinações de moléculas de CO2 . II. A molécula mais leve é o que é encontrado em maior proporção. III. A molécula mais pesada encontrada é o 14C 18O2.
Assinale a alternativa correta .
I. São possíveis 9 combinações de moléculas de CO2 . II. A molécula mais leve é o que é encontrado em maior proporção. III. A molécula mais pesada encontrada é o 14C 18O2.
Assinale a alternativa correta .