Questões de Concurso
Filtrar
3.317 Questões de concurso encontradas
Página 3 de 664
Questões por página:
Questões por página:
Analise as seguintes reações:
I. CH4 (g) + O2 (g) → CO2 (g) + H2O (g)
II. CaO (s) + CO2 (g) → CaCO3 (s)
III. PbCO3 (s) → PbO (s) + CO2 (g)
IV.2N2 (g) + 3H2 (g) → 2NH3 (g)
V. Fe (s) + 2HCl (aq) → FeCl2 (aq) + H2 (g)
Assinale a alternativa que classifica corretamente a reação apresentada.
I. CH4 (g) + O2 (g) → CO2 (g) + H2O (g)
II. CaO (s) + CO2 (g) → CaCO3 (s)
III. PbCO3 (s) → PbO (s) + CO2 (g)
IV.2N2 (g) + 3H2 (g) → 2NH3 (g)
V. Fe (s) + 2HCl (aq) → FeCl2 (aq) + H2 (g)
Assinale a alternativa que classifica corretamente a reação apresentada.
A análise dos dados termodinâmicos de reações permite a previsão da espontaneidade. Na tabela a seguir estão apresentados os dados termodinâmicos de duas reações químicas.
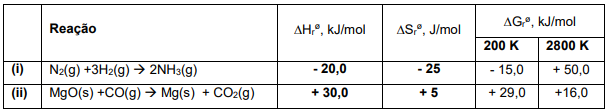
A partir dos dados apresentados, identifique as seguintes afirmativas como verdadeiras (V) ou falsas (F):
( ) A diminuição da temperatura desfavorece a espontaneidade da reação (i). ( ) O aumento da temperatura favorece a espontaneidade da reação (ii). ( ) Na temperatura de 400 K, a reação (i) será espontânea. ( ) Na temperatura de 4000 K, a reação (ii) será espontânea.
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.

A partir dos dados apresentados, identifique as seguintes afirmativas como verdadeiras (V) ou falsas (F):
( ) A diminuição da temperatura desfavorece a espontaneidade da reação (i). ( ) O aumento da temperatura favorece a espontaneidade da reação (ii). ( ) Na temperatura de 400 K, a reação (i) será espontânea. ( ) Na temperatura de 4000 K, a reação (ii) será espontânea.
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.
A retina do olho humano contém dois tipos de células especializadas: os cones e os bastonetes. Nos bastonetes acontece uma transformação química fundamental para a química da visão. Trata-se da conversão do retinol (Vitamina A) em retinal que, na sequência, sofrerá outras transformações.
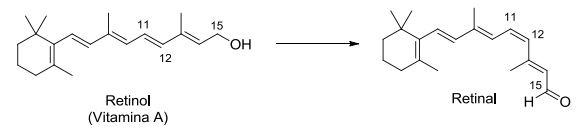
Sobre o tema, considere as seguintes afirmativas:
1. O grupo funcional álcool no retinol é convertido a aldeído no retinal. 2. A ligação dupla entre os carbonos 11 e 12 sofre uma reação de isomerização. 3. A molécula do retinal apresenta um grau de oxidação superior ao do retinol. 4. A molécula do retinol apresenta um centro quiral no carbono 15.
Assinale a alternativa correta.

Sobre o tema, considere as seguintes afirmativas:
1. O grupo funcional álcool no retinol é convertido a aldeído no retinal. 2. A ligação dupla entre os carbonos 11 e 12 sofre uma reação de isomerização. 3. A molécula do retinal apresenta um grau de oxidação superior ao do retinol. 4. A molécula do retinol apresenta um centro quiral no carbono 15.
Assinale a alternativa correta.
A reação de hidrólise da acetilcolina, esquematizada abaixo, é fundamental na transmissão de impulsos nervosos nos seres vivos. A reação é promovida pela enzima acetilcolinesterase (AChE).
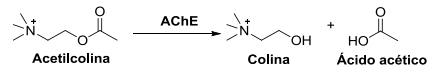
Considere as seguintes afirmativas sobre o papel de AChE nessa reação:
1. AChE é catalisador da reação. 2. AChE aumenta a energia de ativação da reação. 3. AChE promove caminhos reacionais alternativos. 4. AChE inibe a formação de intermediários.
Assinale a alternativa correta.

Considere as seguintes afirmativas sobre o papel de AChE nessa reação:
1. AChE é catalisador da reação. 2. AChE aumenta a energia de ativação da reação. 3. AChE promove caminhos reacionais alternativos. 4. AChE inibe a formação de intermediários.
Assinale a alternativa correta.